制药
直面挑战,确保药品的质量和合规性。
在监管严格的制药领域,质量和安全是指导原则。创新、高效和高质量的产品一直是我们的追求目标,并且符合 FDA 推动的 21 CFR Part 11 及各种药典的要求。我们需要对各种参数进行监测、检查和复查;产生的数据必须是相关、可靠的,并且要符合 ALCOA+ 原则。安东帕在质量和生产控制、研究和开发中有许多解决方案,甚至更好:安东帕在现场认证您新购买的仪器,并在短时间内将其带入您的工作流程。
Anton Paar 产品

Nova

L-Cor 4000

Lyza 3000

Lyza 7000

RST

SAXSpoint 500

SAXSpoint 700

SAXSpace

DMA 35 标准

Abbemat 专业型 7001

Abbemat 专业型 7201

Litesizer DLS 101

Litesizer DLS 301

Litesizer DLS 501

Litesizer DLS 701

DSR502

Litesizer DIA 100

Litesizer DIA 500

Litesizer DIA 700

MCR 703 MultiDrive

L-Cor 6000

PoreMaster

PoreMaster 33

PoreMaster 60

Cora 5001 Fiber 制药版

Cora 5001 Fiber 在线监测

Cora 5001 Fiber 标准版

Cora 5001 Direct 制药版

Cora 5001 Direct 标准版

Abbemat 实用型 3001

Abbemat 实用型 3101

Abbemat 实用型 3201

L-Sonic 5100

L-Dens 3300

L-Dens 7400

L-Dens 7500

L-Rix

制药测量系统

制药测量系统 配置 1

制药测量系统 配置 2

制药测量系统 配置 3
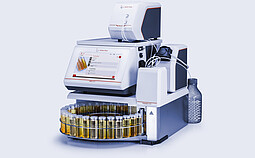
浊度测量系统

聚合物测量系统

聚合物测量系统 配置 1

聚合物测量系统 配置 2

Abbemat 高性能型 5001

Abbemat 高性能型 5101

Abbemat 高性能型 5201

PMA 500
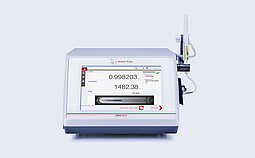
DMA 6002 Sound Velocity

L-Com 5500

Julia DSC 300

Julia DSC 500

Monowave

Monowave 200

Monowave 400

Monowave 450

Multiwave

MCT³

Snap 51

Ultratap 500

Ultratap 500 双站
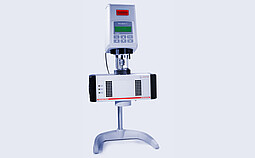
RheolabQC
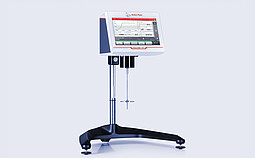
ViscoQC

DMA 4002
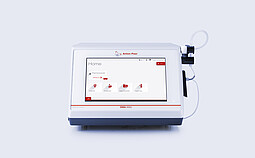
DMA 5002

DMA 6002

MCP

MCR 53

MCR 73

MCR 93

MCP 100

MCP 150

RapidOxy 100

RapidOxy 100 Fuel

MCR 流变仪 + Cora 5001

L-Dens 2300

Litesizer DIF 100

Litesizer DIF 300
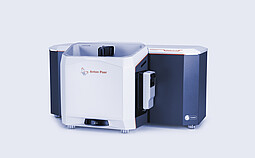
Litesizer DIF 500

TRB³

Ultrapyc

Ultrapyc 7000

Ultrapyc 7000 Micro

TRB V / THT V

L-Cor 8000

DMA 1002

DMA 502

(NHT³)

DMA 1001 EZ

DMA 4101 EZ

DMA 4501 EZ

DMA 5001 EZ

DMA 501 EZ

XRDynamic 500

HTR 7000
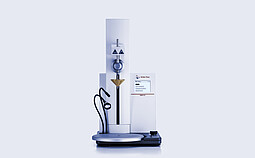
PNR 500
SVM 1001

SVM 1001 Simple Fill
SVM 1101 Simple Fill

UNHT³

L-Cor 8500

SVM 2001

SVM 3001

SVM 3001 Cold Properties

SVM 4001

Autosorb

Autosorb 6100

Autosorb 6200

Autosorb 6300

MCR 703 MultiDrive

MCR 703 Space MultiDrive
通过少量样品检查药物的纯度和功效,
在药物研发和逆向工程中,您往往只需要少量样品。当使用 MCP 系列旋光仪测量旋光度和比旋度时,可以使用长度为 2.5 mm 的旋光管解决这一问题。这些小的旋光管也非常适合测量深色样品。 Modulyzer 等模块系统可在一个周期内针对同一个样品瓶,提供一个既节省空间又节省样品的解决方案用于测量旋光度和折光率。
加速药物研发的库生成
药物研发过程中,同时或顺序合成化合物物质库耗时且昂贵。必须提前优化温度、时间及溶剂、添加剂、催化剂或基体摩尔浓度中的变量等反应参数。此外,在药物研发过程中,所需的产品数量会发生变化。与传统方法相比,采用微波辅助合成可以大幅缩短反应时间。例如,由于节省了典型库生产的预期时间,因此从以往的 37 天减少到只需 2 天。使用安东帕的 Monowave 400 和一个自动化的小瓶处理系统,24个化合物库可以连续合成。 Multiwave PRO 碳化硅板允许多达192个位置的反应筛选。
检查溶液的稳定性
如果滴眼液等溶液中含有团聚体,消费者会反感。可以使用 Litesizer 颗粒分析仪测量 透光率来检查溶液中的团聚体。如果溶液的透光率偏低,产品可能就没有达到市场要求的高标准。
仪器的安装和调试需要 1 至 3 个工作日
其中一点是合规性,即设置和集成一种新的测量仪器,另一点是审计准备。为选定的仪器实施安东帕的制 药资格认证包 ,可在几天内就能认证好您的新仪器并进行运转。此方案涵盖完整仪器认证的所有步骤(DQ、IQ、OQ、PQ、风险分析、21 CFR Part 11 自检清单、偏差列表、追踪溯源和 Word 文件格式的用户 SOP)。此认证方案符合 GMP、21 CFR Part 11、GAMP 5、USP1058> 的要求,可用于后续的再次认证。nbsp
评估温度和湿度对配方引起的变化
在生产过程和储存期间,药物暴露在不适宜的湿度和温度中会发生变化。这些条件可能会导致意外的相变,造成效力发生变化,最坏的情况下甚至会造成负面影响。可以使用非环境 X 射线衍射来研究温度和相对湿度对晶体结构、相变和药物多态样品的影响。在高相对湿度 和不同温度条件下,可以采用安东帕的 CHC plus+ Cryo 和湿度箱记录 X 射线衍射数据。按照露点曲线,湿度箱的湿度可以在恒定的温度下发生变化,温度也可在恒定的湿度下发生变化。