의약품
의약 제품의 품질 및 규정 준수를 보장하는 문제에 대응
규제가 고도화된 의약 부문에서는 품질과 안전성이 지침이 됩니다. 혁신, 고효율성, 최고 품질의 제품은 항상 FDA는 물론 여러 약전에서 주도하는 21 CFR Part 11 요구 사항을 준수합니다. 다양한 파라미터를 모니터링, 확인, 그리고 관리할 필요가 있습니다. Anton Paar에는 연구 개발 분야에서 품질 및 생산 관리에 사용할 수 있는 여러 뛰어난 솔루션이 있습니다. Anton Paar의 장비는 단시간에 현장에서 새로 구입한 장비를 검증하고 사용할 수 있습니다.
Anton Paar 제품

Nova

L-Cor 4000

Lyza 3000

Lyza 7000

PMA 500


SAXSpoint 500

SAXSpoint 700

SAXSpace

Autosorb

Autosorb 6100

Autosorb 6200

Autosorb 6300

NHT³

제약 측정 시스템

제약 측정 시스템 구성 1

제약 측정 시스템 구성 2

제약 측정 시스템 구성 3
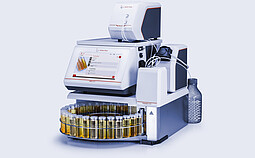
탁도 측정 시스템

폴리머 측정 시스템

폴리머 측정 시스템 구성 1

폴리머 측정 시스템 구성 2

Litesizer DLS 101

Litesizer DLS 301

Litesizer DLS 501

Litesizer DLS 701

MCR 703 MultiDrive

Litesizer DIA 100

Litesizer DIA 500

Litesizer DIA 700

DSR 502

SVM 2001

SVM 3001

SVM 3001 Cold Properties

SVM 4001

Cora 5001 Fiber 공정 모니터링

Cora 5001 Fiber 제약

Cora 5001 Fiber 표준

Litesizer DIF 100

Litesizer DIF 300
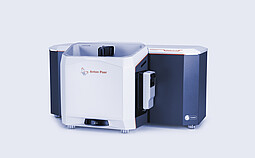
Litesizer DIF 500

MCT³

Monowave

Monowave 200

Monowave 400

Monowave 450

Multiwave

MCP 100

MCP 150

DMA 4002
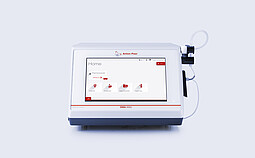
DMA 5002

DMA 6002

MCP

L-Com 5500
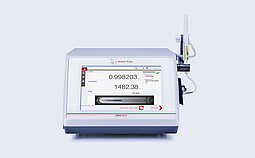
DMA 6002 음속 측정기

Ultrapyc

Ultrapyc 7000

Ultrapyc 7000 Micro

Abbemat Essential 3001

Abbemat Essential 3101

Abbemat Essential 3201

MCR 53

MCR 73

MCR 93

RapidOxy 100

RapidOxy 100 Fuel

Cora 5001 Direct 제약

Cora 5001 Direct 표준

PoreMaster

PoreMaster 33

PoreMaster 60

Julia DSC 300

Julia DSC 500

Abbemat Advanced 5001

Abbemat Advanced 5101

Abbemat Advanced 5201

L-Dens 2300

UNHT³

L-Cor 6000

MCR 레오미터 + Cora 5001

L-Rix

L-Dens 3300

L-Dens 7400

L-Dens 7500

L-Sonic 5100

XRDynamic 500
SVM 1001

SVM 1001 Simple Fill
SVM 1101 Simple Fill
PNR 500

HTR 7000

Abbemat Pharma 7001

Abbemat Pharma 7201

TRB V / THT V

MCR 703 MultiDrive

MCR 703 Space MultiDrive

L-Cor 8500

L-Cor 8000

DMA 1002

DMA 502

Ultratap 500

Ultratap 500 Twin

TRB³

DMA 1001 EZ

DMA 4101 EZ

DMA 4501 EZ

DMA 5001 EZ

DMA 501 EZ
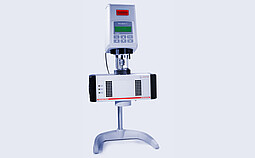
RheolabQC
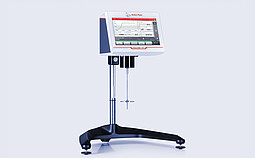
ViscoQC

DMA 35 표준

Snap 51
소량의 시료로 약물의 순도와 효능 확인
신약 개발 및 역공학에서 작업해야 하는 시료는 대부분 소량입니다. MCP 시리즈의 파라미터를 사용하여 선광도 또는 특정 회전을 측정하는 경우 이 문제는 2.5mm 길이의 시료 셀을 사용하면 해결됩니다. 이러한 소형 셀은 색상이 어두운 시료의 측정에도 매우 적합합니다. Modulyzer와 같은 모듈식 시스템은 동일한 시료 바이알에서 선광도 및 굴절률 모두를 측정하기 위한 공간 및 시료 절감 솔루션을 제공합니다.
신약 개발을 위한 라이브러리 생성 가속화
신약 개발을 위해합성된 물질의 화합물 라이브러리를 생성하는 데는 오랜 시간과 많은 비용이 소요됩니다. 솔벤트, 첨가제, 촉매제의 온도, 시간 및 변화 또는 기질의 몰 비율과 같은 반응 파라미터가 미리 최적화되어야 합니다. 또한, 신약 개발 프로세스 중에 필요한 제품 수량이 변경됩니다. 마이크로파형 합성을 사용하면 기존 가열에 비해 반응 시간을 최소화할 수 있습니다. 일반적인 라이브러리 생성을 위한 예상 시간이 절감되어 예를 들어, 일반적으로 소요되는 기간이 37일에서 단 이틀로 단축됩니다. 자동 바이알 취급 시스템을 포함하는 Anton Paar의 Monowave 400을 사용하면 이후에 24개 화합물 라이브러리를 합성할 수 있습니다. 탄화 규소판을 포함하는 Multiwave PRO를 사용하여 최대 192개 위치의 반응 검사를 수행할 수 있습니다.
용액의 안정성 확인
소비자는 안약과 같은 용액에 응집체가 포함된다면 불쾌할 것입니다. 용액에 응집체가 있는지 확인하려면 Litesizer 입도 분석기를 사용하여 투과율을 측정할 수 있습니다. 용액의 투과율이 낮으면 제품은 시장에서 요구하는 높은 수준을 충족할 수 없을지도 모릅니다.
기기는 하루 내지 사흘 안에 설치 및 검증, 작동할 수 있습니다.
규정 준수는 기기 사용 시 고려해야할 필수 사항이며, 새로운 기기의 설정, 통합, 감사 준비도 또한 고려해야 할 사항중 하나입니다. 선택한 장비에 대한 Anton Paar의 제약 규격 인증 패키지를 이용하면 며칠 안에 새 기기를 가동할 수 있습니다. 전체 장비 적격 심사의 모든 단계를 포함합니다(DQ, IQ, OQ, PQ, 위험 분석, 21 CFR Part 11 체크리스트, 편차 목록, 추적 가능성 매트릭스, 사용자 SOP Word 파일). 이 패키지는 GMP, 21 CFR Part 11, GAMP 5, USP <1058>의 요구 사항을 충족하고 이후 규격 재인증에 사용할 수 있습니다.
약제에 대한 온도 및 습도 유도 변경 사항 평가
의약품은 생산 공정 및 보관 중에 습도 및 온도 변화를 겪을 수 있습니다. 이러한 조건은 예기치 못한 상 전이로 이어져 결과적으로 효능 변화 또는 최악의 경우 부작용이 발생할 수 있습니다. 약물의 결정 구조, 상 전이, 다형성에 대한 온도 및 상대 습도의 영향은 비 상온 X-선 회절을 사용하여 조사할 수 있습니다. Anton Paar의 CHC plus+ 극저온 및 습도 챔버를 활용하면 높은 상대 습도 및 다양한 온도에서 X-선 회절 데이터를 기록할 수 있습니다. 챔버를 사용하면 이슬점 곡선에 따라 일정한 온도에서 습도를 변화시킬 수 있으며 일정한 습도에서 온도를 변화시킬 수도 있습니다.