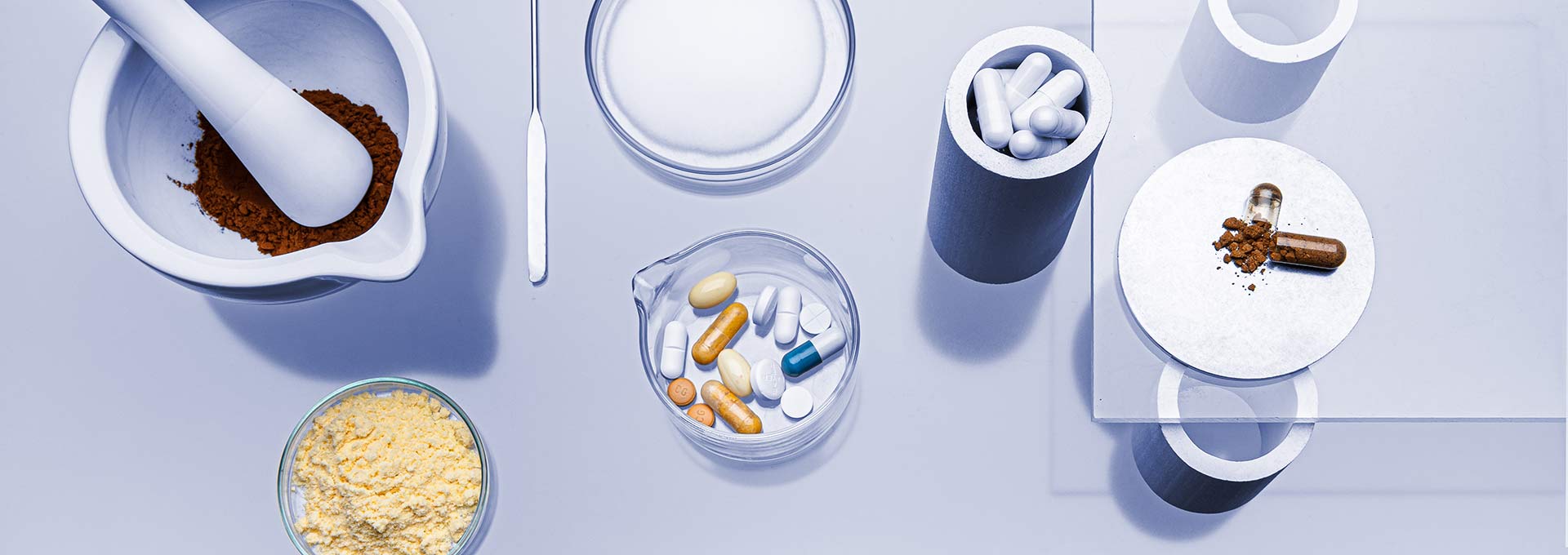
Akışkanlık, çözünürlük, tutarlılık, saflık ve stabilite, farmasötik tozların optimize edilmesi söz konusu olduğunda dikkate alınması gereken parametrelerdir. Gerçek koşullar altında farmasötik toz karakterizasyonuna odaklanan geniş bir analitik cihaz yelpazesi, ürünün etkinliğini artırmanıza yardımcı olacaktır.
Parçacık özellikleri konusundaki kavrayışınızı derinleştirmek, daha öngörülebilir formülasyonlara yol açar. Formülasyondan üretime kadar her adımda tozlarınızın akış davranışını anlayın. Dikkate alınmayan çevre koşullarının üretim verimliliğini ve kalitesini etkilemesini önleyin.
Yüzey alanı, parçacık boyutu ve dağılımı, genel ve sıkıştırılmış yoğunluk, toz akış özellikleri ve daha fazlası gibi parametreler için güvenilir ve tekrarlanabilir sonuçlar elde edin. X-ışını difraksiyonu yoluyla ortam dışı sıcaklıklarda polimorf özellikler hakkında bilgi edinin. Raman spektroskopisi ile aktif farmasötik bileşenleri ve eksipiyanları tanımlayın. Kapalı kap yakma sistemi yoluyla endüktif olarak eşleştirilmiş plazma kütle spektrometrisi için numunelerinizi hazırlayın.
"Farmasötik Toz Karakterizasyonu İçin Alan Kılavuzu" e-kitabını indirin ve daha fazlasını öğrenin.

Okunması Gereken Anton Paar E-Kitabı: “Farmasötik Toz Karakterizasyonu İçin Saha Kılavuzu”
Malzemeler hakkındaki anlayışınızı derinleştirin ve farmasötik tozları kontrol edin. Farmasötik toz karakterizasyonuna odaklanan ve gerçek ölçüm verilerini içeren bu e-kitap, gerçek yaşam koşulları altında akışkanlık, çözünürlük ve tutarlılık gibi farmasötik toz zorluklarıyla nasıl başa çıkacağınızı anlatır.
Çözünürlük, Çözünme Oranları ve Tutarlılık

İlaç formülasyonu tutarlılığını, çözünme oranlarını, biyoyararlılık ve nihai absorpsiyon davranışını optimize etmek, ilaç geliştirme, test etme ve uygulama sırasında kritik öneme sahiptir. Bu parametrelerin her birini doğrudan etkileyen birincil fiziksel özelliklerden biri, formülasyonun parçacık boyutudur. Bir ilaç formülasyonunun parçacık boyutunun ve boyut dağılımının ve bunun zaman içinde ve farklı koşullar altında nasıl değiştiğinin hızlı ve doğru bir şekilde ölçülmesi, genellikle yeni bir formülasyon geliştirmenin ilk adımıdır.
Ek olarak, bir toz farmasötik formülasyonun yüzey alanı ve gözenekliliği, özellikle çözünürlük ve çözünme oranları hakkında daha fazla bilgi sağlar. Spesifik olarak: genel yüzey alanı ne kadar büyükse ve bir tozda ne kadar fazla gözenek bulunursa, çözünürlük ve çözünme hızı o kadar iyi olur. Farmasötik tozların partikül boyutunun yanı sıra yüzey alanı ve gözenekliliğinin doğru bir şekilde ölçülmesi, ilaç tutarlılığını ve dağıtımını optimize etmek için kritik öneme sahiptir. Hastada ilacın salım hızının kontrol edilmesi için de önemlidir.
Toz Akışı

Tozların endüstriyel ölçekte işlenmesi, taşınması ve depolanması, tipik olarak pilot ölçekte görülmeyen sorunlara neden olur. Pek çok toz, maruz kaldıkları çevresel koşullara (örneğin, sıcaklık ve nem) önemli bir davranışsal bağımlılık gösterir. Bu davranış değişiklikleri kendilerini akışkanlık, kohezyon, aglomerasyon eğilimi ve daha birçok özellikteki değişiklikler olarak ifade eder. Bu genellikle istenmeyen etkiler, örneğin eksipiyan ve aktif farmasötik bileşenler ayrıldığında veya ayrıştığında sorunlu olabilir. Akış özelliklerindeki bu değişiklik, işleme ve doldurma sırasında bir zorluk teşkil edebilir.
Sıcaklık/neme bağlı toz reolojik özelliklerinin belirlenmesi, farmasötik tozların akış ve mekanik davranışlarının karakterize edilmesini sağlar. Toz formülasyonlarınızı analiz edin ve doğru hazırlama koşullarını belirlediğinizden emin olun. Verimli ve kusursuz taşıma, işleme ve karıştırma için toz reolojisi ile akış özelliklerini anlayın.
Paketleme ve Tablet Oluşturma
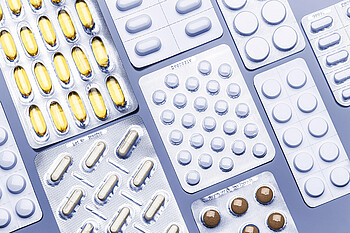
Katı yoğunluğu, farmasötik tozların – ilaçlar veya eksipiyanlar – önemli bir özelliğidir. Genel ve sıkıştırılmış yoğunluk, tozun akış özellikleri ile ilgilidir. Bir tozun, özellikle bir katkı maddesinin veya eksipiyanın akışkanlığı, bu katkı maddesinin granülasyon veya tablet oluşturma sürecini nasıl etkileyeceğini belirlemede önemlidir. İyi akışkanlık; tutarlı ağırlık ve dozajın elde edilmesi için kapsüllerin uygun, tek tip doldurulmasını sağlar.
Bir tabletin açık gözenekliliğinin belirlenmesi, dayanıklılık ve raf ömrü dahil olmak üzere birçok farklı tablet özelliğini anlamak için kritik öneme sahiptir. Gözeneklilik, tablet kompresyonu sırasında eksipiyan kırılmasının önlenmesinde de önemlidir.
Gaz piknometrisi ölçümleri, toz akış bilgilerini ve tablet gözenekliliğini değerlendirmenize izin veren iskelet yoğunluğu verileri sağlar.
Saflık, Kararlılık ve Kristallik Yüzdesi (XRD ve SAXS)

Farmasötik tozların uzun vadeli stabilitesi ve örneğin saklama koşullarının ve paketlemenin bu tür tozların stabilitesini nasıl etkilediği kilit önemdedir. X-ışını difraksiyonu (XRD) ve küçük açılı X-ışını saçılımı (SAXS) gibi yöntemler, kristallik derecesini (amorf parçalar ve kristal fazlar arasındaki oran) değiştiren veya başka yapısal değişiklikler oluşturan eskime etkileri için tozları analiz etmek amacıyla kullanılabilir. Bunlar zamanla ve tozların saklama koşullarına göre önemli ölçüde değişecektir. SAXS ve XRD, numuneleri ortam ve ortam dışı koşullar altında (ve gerektiğinde yerinde) ölçebilir ve eskime, stabilite, uygun paketleme ve optimum saklama koşulları hakkında temel bilgiler verir.
Herhangi bir aktif farmasötik bileşenin (API) kristal yapısı, ürün stabilitesini, çözünürlüğü ve nihayetinde biyoyararlılığı belirler. XRD, bir tozda bulunan formları anlamak için kristal fazları tanımlamanın ve API'lerin polimorf taramasını gerçekleştirmenin standart yöntemidir.
Elemental Saflık Analizi İçin Örnek Hazırlama

Elemental safsızlıklar sadece hasta için toksikolojik bir risk oluşturmadığından ve farmasötik ürünlerin kalite ve etkinliğini de etkileyebileceğinden; bunların analizi, farmasötiklerin geliştirilmesi ve kalite kontrolünde önemli bir rol oynamaktadır.
Elemental safsızlıkların miktarı, mikrodalga destekli asitle parçalama gibi güvenilir numune hazırlama teknikleriyle birlikte ICP-OES veya ICP MS aracılığıyla gerçekleştirilir. Bu özel numune hazırlama yönteminin kullanılması, mükemmel geri kazanım oranları, düşük varyasyonlar ve yüksek numune verimi sağlar.
Örnek Tanımlama Bilgisi
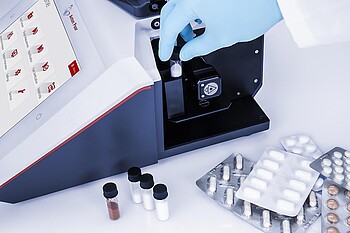
İlaç üretim endüstrisi, en sıkı şekilde düzenlenen küresel pazarlardan biridir. Bu, ürün kalitesini garanti eder ve dünya çapında hastalar için riskleri en aza indirir. Tüm API'ler, eksipiyanlar, ilaç ürünleri ve ambalaj malzemeleri için uluslararası ilaç kodeksleri ve GMP yönergeleri kapsamında kimlik testleri gereklidir. ABD İlaç Kodeksi 197 ve 858 bölümlerine göre, kimlik testleri Raman spektroskopisi kullanılarak yapılabilir ve USP 1225'e göre doğrulanmalıdır.
Bir serinin daha fazla kullanıma uygun olup olmadığını veya reddedilmesi gerekip gerekmediğini hızlı bir şekilde değerlendirmek için hızlı ve doğru yöntemler gereklidir. Kimlik testi çözümleri, FDA'nın CFR 21 Bölüm 11'ine uygun olmalı, veri bütünlüğü ve eksiksiz bir denetim izi sağlanmalıdır.